La malattia di Alzheimer rappresenta il 70% delle malattie neurodegenerative. Questa complessa patologia è caratterizzata da una lenta ma progressiva evoluzione delle facoltà cognitive (memoria, linguaggio, ragionamento, attenzione), riducendo progressivamente l’autonomia dei soggetti affetti. Se la sua origine è multifattoriale, i ricercatori stimano che un caso su tre potrebbe essere evitato grazie all’adozione di uno stile di vita migliore. In Francia ne sono colpite un milione di persone, soprattutto donne. E, con l’invecchiamento della popolazione, prevediamo che il numero di casi triplicherà entro il 2050. C’è quindi un’urgente necessità di far avanzare la ricerca. Soprattutto perché gli unici farmaci finora disponibili non curano la malattia ma ne rallentano i sintomi, con scarsi miglioramenti nelle condizioni del paziente.
L’arrivo sul mercato di molecole con finalità curative segna quindi una svolta. Il 14 novembre l’Agenzia europea per i medicinali ha autorizzato la commercializzazione del lecanemab (Leqembi), del laboratorio giapponese Eisai e del produttore americano Biogen. Non è ancora distribuito in Francia, ma l’Eisai presenterà una richiesta di accesso anticipato affinché i pazienti possano beneficiarne mentre l’Alta Autorità della Sanità si pronuncia sulla sua commercializzazione. La molecola potrà poi essere prescritta da specialisti, in particolare neurologi, in centri e servizi appositi.
La patologia si manifesta con l’accumulo intorno ai neuroni di placche costituite da proteine anomale, beta-amiloide e tau, che alterano la connessione tra le cellule neuronali, portandole alla morte. “Il trattamento utilizza l’immunoterapia: un anticorpo monoclonale, prodotto mediante ingegneria genetica, che prende di mira le placche amiloidi come un missile balistico e le distrugge. L’obiettivo è arrestare il processo progressivo della malattia per consentire al paziente di ritrovare una qualità di vita accettabile”, spiega il dottor Riadh Caïd-Essebsi, presidente del consiglio medico dell’Ospedale Americano di Parigi.
“L’obiettivo è fermare la progressione della malattia per riportare il paziente a una qualità di vita accettabile”
Accesso molto controllato al trattamento
Il resto dopo questo annuncio
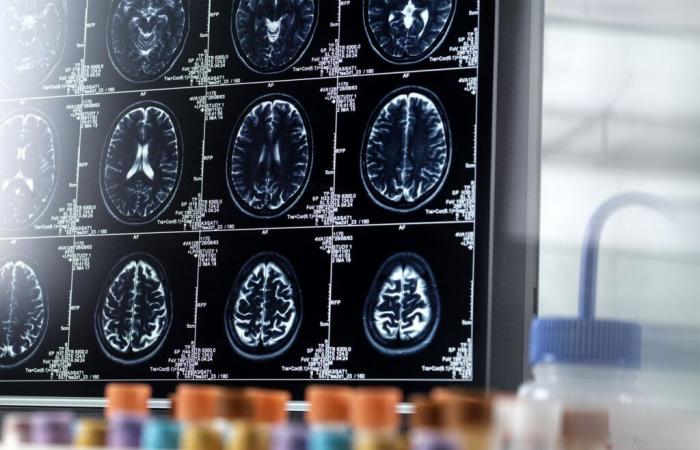
Somministrato per via endovenosa ogni due settimane, il lecanemab riduce il carico di amiloide del 70%. Esponendo il rischio di edema cerebrale ed emorragia che può essere fatale, è riservato a pazienti selezionati che non hanno nessuno, o solo una copia, della variante genetica ApoE4, nota per promuovere effetti collaterali. Questo rischio è purtroppo comune poiché solo dal 5% al 15% dei pazienti sono idonei al trattamento. Questi ultimi devono essere sottoposti a risonanza magnetica prima di iniziare Leqembi, nonché prima di assumere la 5a, 7a e 14a dose e in qualsiasi momento in caso di sintomo allarmante per consentire la diagnosi precoce di una lesione.
Altre molecole in futuro
Con un meccanismo d’azione simile, nel 2025 è atteso il donanemab (Kisunla). Il laboratorio americano Eli Lilly, che lo produce, annuncia risultati superiori a Leqembi. “Stiamo entrando in una nuova era farmacologica con cure ancora imperfette ma che permettono di offrire una soluzione ai pazienti che sono all’inizio della loro malattia. Tuttavia, queste immunoterapie sono costose. Da vedere se l’azienda è pronta a sostenere il costo di questo trattamento, che ammonta a 26.000 euro all’anno! » indica il dottor Caïd-Essebi. Ma la ricerca sta procedendo rapidamente. Sono in fase di studio le molecole che prendono di mira la proteina tau. Così come i farmaci antiobesità, che prevengono la senescenza cerebrale agendo sull’infiammazione. In futuro la soluzione sarà senza dubbio una combinazione di trattamenti.
Health